一个模型,统治所有分子 | 清华&字节跳动发布AnewOmni,首次实现从小分子到纳米抗体的跨模态全原子药物设计
一个模型,统治所有分子 | 清华&字节跳动发布AnewOmni,首次实现从小分子到纳米抗体的跨模态全原子药物设计

MindDance
发布于 2026-03-31 17:39:47
发布于 2026-03-31 17:39:47
从分裂走向统一:分子设计的一个根本性问题
生物分子相互作用是细胞生命活动的核心。小到一颗药物分子与蛋白口袋的结合,大到一枚纳米抗体对肿瘤抗原的识别,本质上都遵循同一套原子尺度的物理化学原理——氢键、疏水作用、范德华力、静电相互作用。然而在实际药物开发中,小分子、多肽、抗体的设计方法却各成体系,采用截然不同的表示方式、规则和流程。这种分裂并非源于分子识别机制本身的差异,而更多反映了化学与生物学技术的历史演进路径。
近年来,结构导向的生成模型在各个模态上都取得了长足进步。TargetDiff、DrugFlow 等模型在小分子生成上表现不俗,RFDiffusion 在蛋白质设计中大放异彩,DiffAb 则专注于抗体的CDR区域设计。但这些方法几乎都绑定在单一模态之上,无法跨模态迁移,更谈不上生成训练分布之外的非典型化学结构,如非标准氨基酸或大环分子。
一些试图跨越模态边界的工作已经出现。例如 BoltzGen 和 ODesign 用氨基酸级别的token表示蛋白质、原子级别的token表示小分子,存在粒度不一致的问题,限制了原子级相互作用模式的迁移。PocketXMol 则走到另一个极端,把所有模态都视为纯原子图——虽然捕捉到了精细的相互作用,却忽略了进化塑造的高阶结构先验(如氨基酸的重复模式),导致它难以扩展到抗体等大型分子。
这就引出了一个核心问题:是否存在一种生成框架,既能在原子层面保留可迁移的相互作用原则,又能保持各模态所需的结构先验,从而实现跨越极大尺度差异的分子设计?
清华大学与字节跳动 AI Drug Discovery 团队的这篇最新工作给出了肯定的回答。他们提出了 AnewOmni——一个在超过500万个生物分子复合物上训练的全原子生成基础模型,首次在同一个框架内实现了小分子、多肽和抗体的统一设计,并在 KRAS G12D 和 PCSK9 两个极具挑战性的靶点上通过湿实验验证了全尺度的设计能力。
AnewOmni 的核心设计:原子到构建模块的分层表示
AnewOmni 的架构核心,是一套被称为 atom-to-block 的分层表示体系,它精妙地平衡了原子级精度和结构级先验知识。
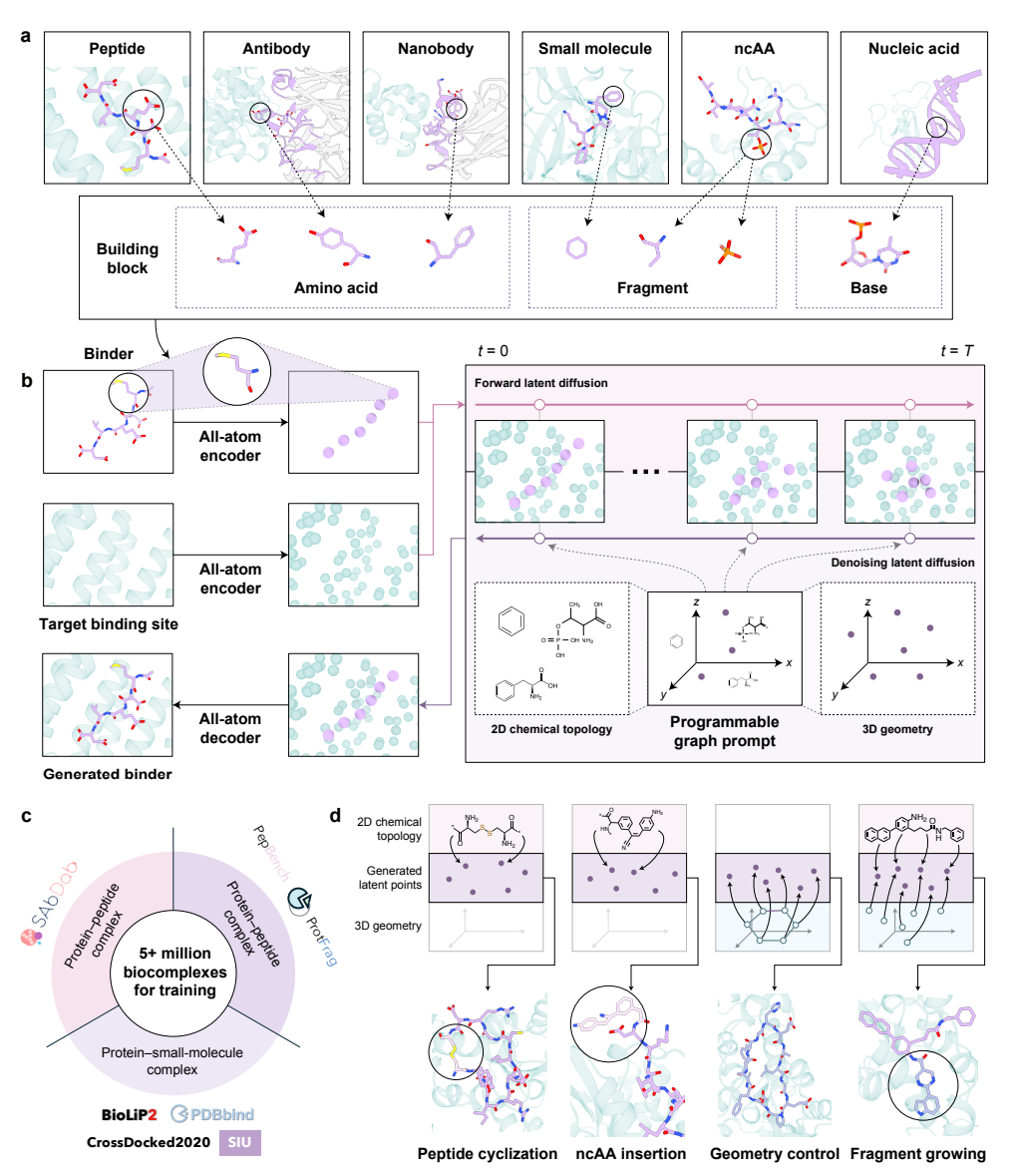
AnewOmni 的整体框架概览
AnewOmni 的整体框架概览
在构建模块的定义上,模型保留了所有标准的生物分子单元,包括20种标准氨基酸和核苷酸碱基。其他化学实体——如小分子和非标准氨基酸——则被分解为从 ChEMBL 数据库中挖掘出的高频分子片段。罕见的子结构会被进一步分解为单个原子,以确保对任意化学空间的完整覆盖。
在这套表示之上,模型由四个核心组件构成。首先是一个全原子变分自编码器(VAE),它负责在原子级分子结构和紧凑的构建模块级潜在表示之间建立可逆映射。每个构建模块被编码为一个潜在嵌入 h ∈ ℝᵈ 和一个空间坐标 x̃ ∈ ℝ³,形成一个连续的潜在点云,其中既压缩了化学先验,也保留了上下文感知的原子级几何信息。
分子生成过程则被交给一个潜在扩散模型——它在压缩后的光滑潜在空间中运行扩散过程,以靶标结合位点的原子环境为条件进行生成。VAE和扩散模型均采用等变Transformer参数化,在保留几何对称性的同时兼容标准Transformer架构,以支持大规模训练。
最后,模型实现了沿生成轨迹的精确似然估计,作为无监督的、模态无关的自排序指标。论文指出,他们也尝试过 AlphaFold3 风格的有监督置信度头来预测成对距离误差,但发现这种置信度估计容易在已见分子分布上过拟合,对未见靶标的泛化能力较差,因此最终选择了无监督似然作为候选分子排序的主要标准。
可编程图提示:无需重新训练的灵活控制
对于实际的药物设计,生成只是第一步——研发人员往往需要对生成过程施加精确的化学和几何约束。AnewOmni 为此引入了可编程图提示(Programmable Graph Prompts)机制,将各种格式的化学和空间约束编码为潜在点云上的节点级或边级条件,直接引导扩散过程的去噪方向。
这一设计的表达能力非常强大。用户可以为指定的潜在点分配任意化学结构作为节点标签,定义它们之间的连接关系作为边标签,还可以指定空间坐标来引导近似定位。所有这些元素可以自由组合成更复杂的约束图,无需重新训练模型即可适配各种设计需求。
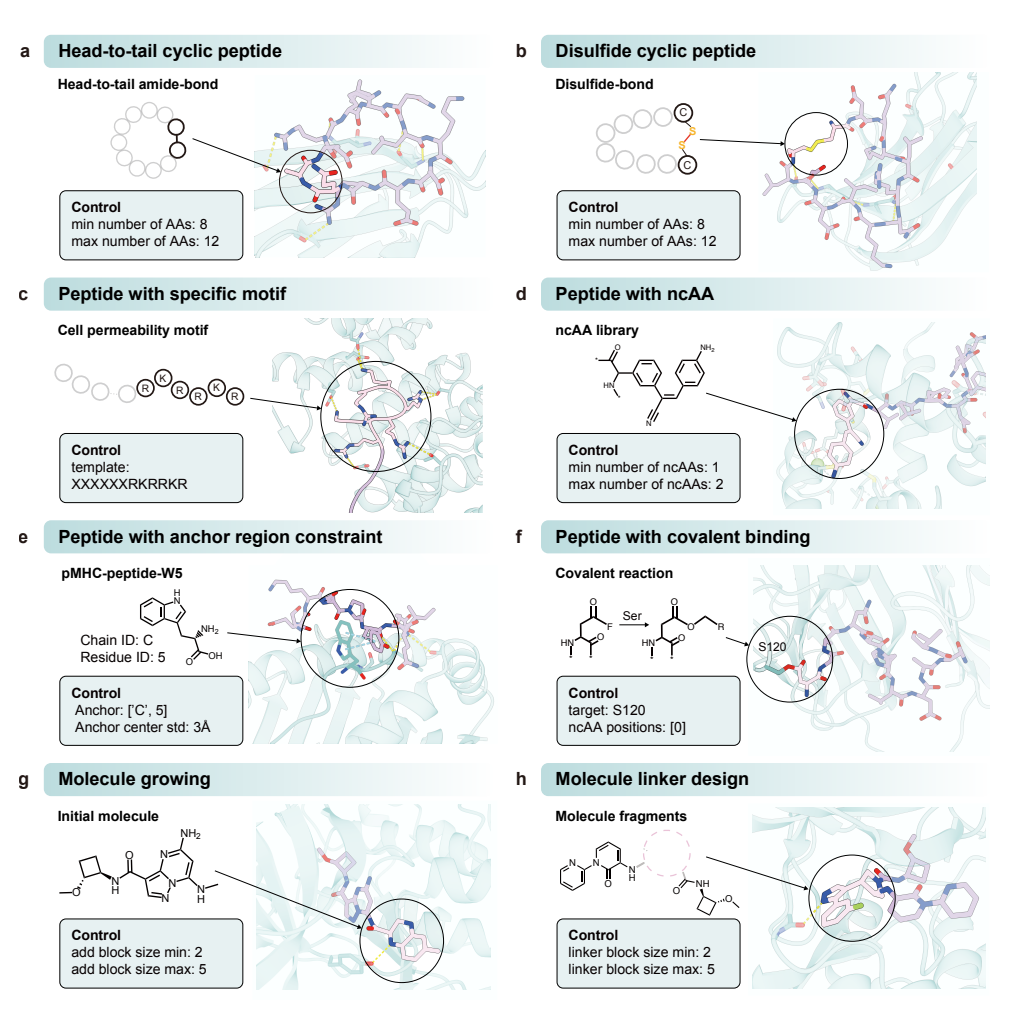
AnewOmni 的可编程设计示例
AnewOmni 的可编程设计示例
论文展示了一系列具体场景。在拓扑控制方面,通过在末端构建模块之间指定一个酰胺键的边级提示,模型便能生成化学上有效的头尾成环肽;通过约束半胱氨酸残基的存在(节点级提示)并强制二硫键连接(边级提示),模型则生成了二硫键稳定的环肽。在化学组成控制方面,将已知的细胞穿透性基序编码为节点级提示后,模型在保留该特定序列模式的同时优化了其三维空间位置,使得生成的多肽在约束基序周围与靶标形成了有利的相互作用。更具挑战性的场景是非标准氨基酸(ncAA)的引入——论文以一种在构象限制下才会发出荧光的ncAA为例,将其应用于钙调蛋白靶标,展示了设计钙离子传感器的可能性。
在相互作用模式控制方面,通过对潜在点施加空间提示,可以将生成偏向于用户指定的锚点区域,这对于需要接触特定锚点残基的 pMHC-多肽识别等场景尤为有用。此外,论文还展示了通过指定反应性ncAA和共价键约束来设计共价结合多肽的能力——以TL1A靶标为例,在其Ser120位点上生成了满足共价反应几何的多肽。最后,模型的可编程性自然延伸到了分子生长和连接子设计,通过固定已有骨架的潜在点并让剩余部分自由生成,实现了基于现有片段的结构扩展。
跨模态训练的收益:一加一大于二
AnewOmni 的一个关键发现是:跨模态联合训练不仅不会损害各模态的性能,反而带来了显著的互惠增益。这一结论得到了多个层面的支撑。
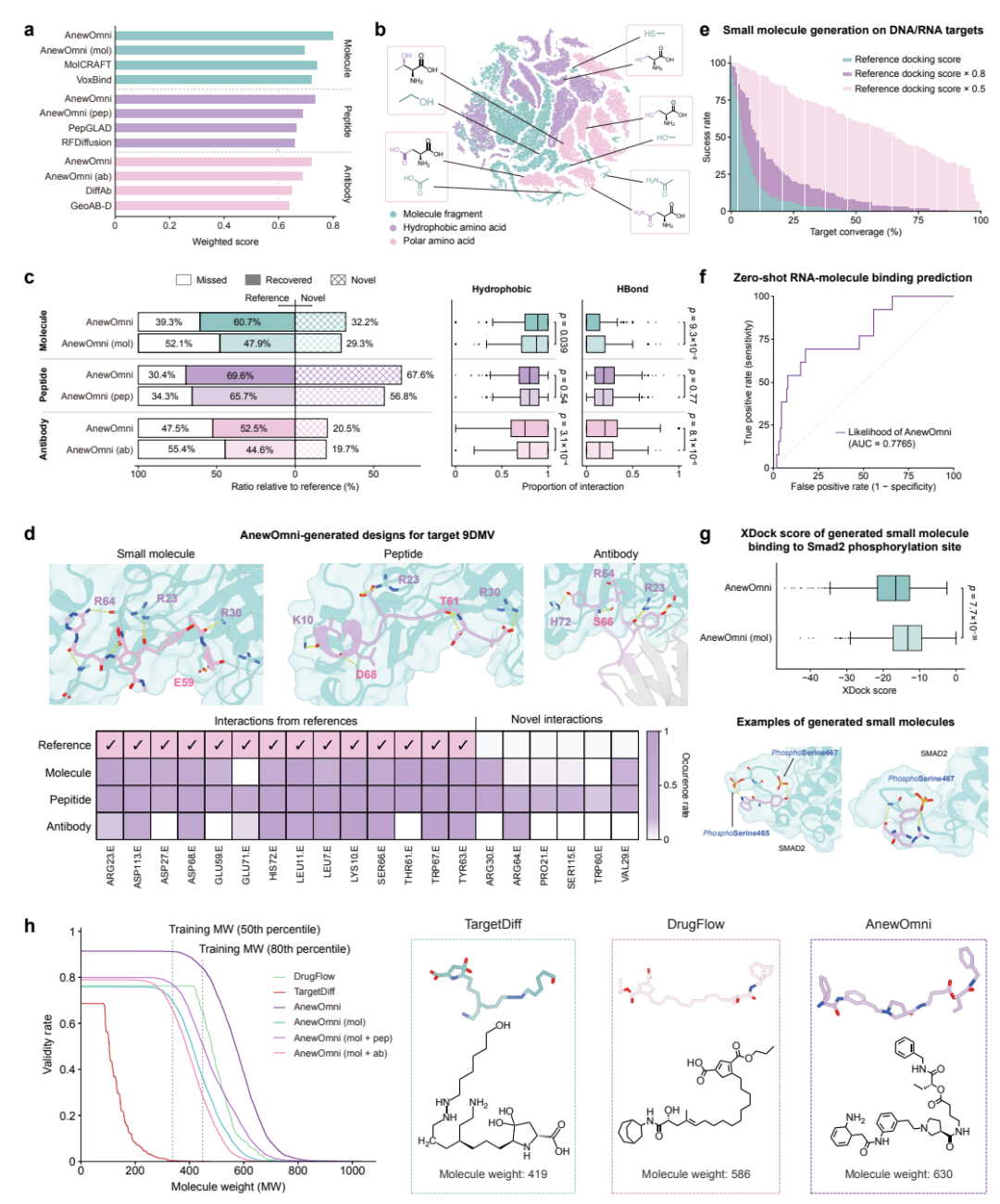
在公开基准测试中,团队将来自统计力场的结合能、理化有效性和分布保真度等互补指标归一化后,聚合为一个0到1之间的综合评分。在小分子、多肽和抗体三个任务上,AnewOmni 统一模型全面超越了各自领域的专用SOTA基线(包括 MolCRAFT、VoxBind、PepGLAD、RFDiffusion、DiffAb、GeoAB-D),也超越了其仅用单模态数据训练的消融版本。
潜在空间的可视化进一步揭示了有意义的组织结构:疏水氨基酸和极性氨基酸以清晰的边界分离,而小分子片段则与功能相似的氨基酸自然融合。具体来说,硫甲基基团与半胱氨酸紧密对齐,羟甲基与丝氨酸聚类,乙酰胺基与天冬酰胺聚类,乙酸基团与天冬氨酸聚类,羟乙基与苏氨酸聚类。这种组织方式反映了模型确实学到了不同构建模块在分子识别中的功能相似性——而这正是跨模态迁移学习的化学基础。
为了更深入地分析跨模态训练如何塑造学到的相互作用模式,研究团队选取了八个近期发布的靶标,让 AnewOmni 对同一结合位点分别生成小分子、多肽和抗体。通过 ProLIF 工具检测分子间相互作用后发现,生成的复合物能够恢复50%–70%的天然相互作用,其中多肽展现出最高的灵活性,既恢复了最多的天然接触,也引入了最多的新型相互作用。跨模态训练使所有模态的相互作用恢复率都得到提升,尤其是小分子和抗体获益最大——比各自的单模态版本多恢复了约10%的天然相互作用。
有趣的是,跨模态训练使小分子更多地依赖疏水相互作用(这本是抗体识别的特征),而抗体则展现出相反的转变,多肽的相互作用偏好变化最小。论文据此推测,多肽可能充当了小分子和抗体之间知识迁移的桥梁角色。
零样本泛化:从未见过核酸,却能为其设计配体
AnewOmni 的训练数据中不包含任何核酸相关复合物。然而,当研究团队收集了139个RNA/DNA靶标并让模型生成小分子结合物时,结果却出人意料地好。
使用物理能量函数 XDock 评估后发现,几乎所有靶标在100次生成内都产生了至少一个结合能超过天然结合物50%的候选分子;在更严格的80%阈值下,70%–80%的靶标仍能产出令人满意的候选物;而对于50%–60%的靶标,模型甚至能生成与天然配体结合能相当的强结合物。
更令人印象深刻的测试来自一个最近发表的、经实验验证的RNA–小分子数据集。研究团队控制 AnewOmni 精确生成该数据集中的同一批分子用于似然估计。在训练过程中完全未见任何 RNA–小分子数据的情况下,模型的生成似然达到了 AUC-ROC 0.7765——仅凭生成概率就能在一定程度上区分结合与非结合的配体-RNA对。
此外,模型在糖基化位点和磷酸化位点等非常规靶标上也展示了零样本生成能力,且相比单模态版本具有显著优势。在分子物理有效性方面,即使分子量远超传统小分子的范围,AnewOmni 依然保持了较高的 PoseBusters 有效性,显著优于 TargetDiff 和 DrugFlow 等基线。消融实验进一步表明,加入多肽或抗体数据均各自贡献了有效性的提升——这种大分子生成能力对于靶向蛋白-蛋白相互作用的延伸结合位点尤为关键。
实验验证一:同一个口袋,三种模态,攻克 KRAS G12D
KRAS 突变存在于超过30%的人类癌症中,其中 G12D 突变是最常见的变体。由于 KRAS 对 GDP 和 GTP 的高亲和力,加上缺乏深且持久的可配体化口袋,它长期被视为经典的不可成药靶点,直到近年来 MRTX1133 的突破性进展。但即便如此,绝大多数后续工作仍然聚焦于 MRTX1133 的 pyrido[4,3-d]pyrimidine 骨架衍生物优化,而该骨架在临床转化中面临生物利用度低的问题。
研究团队将 AnewOmni 部署到了一个极具雄心的实验设计上:用同一个模型,针对 GDP 结合态 KRAS G12D 的同一个 Switch II 口袋,分别设计小分子、多肽和纳米抗体三种完全不同模态的结合物。
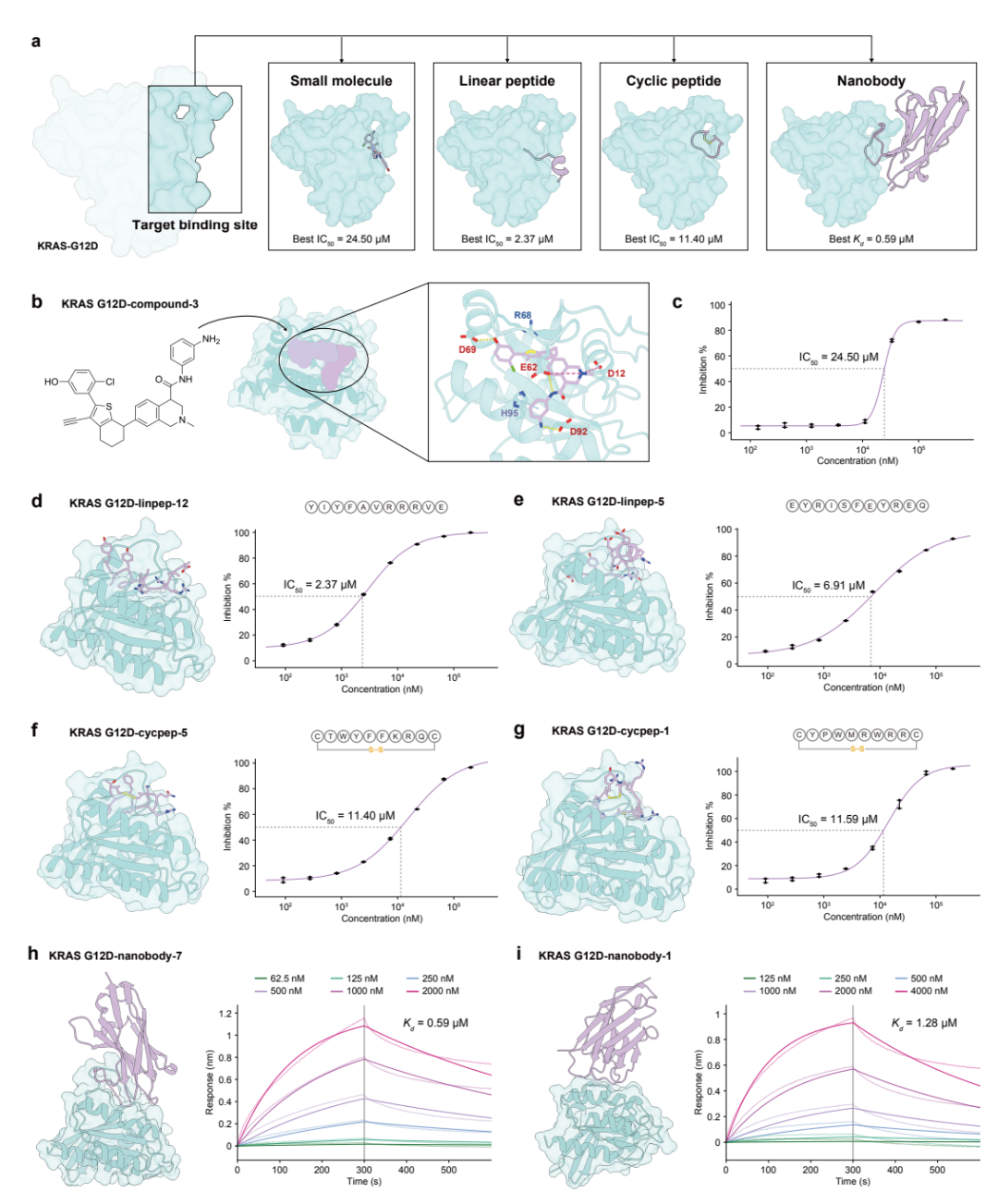
小分子设计。 团队利用 AnewOmni 进行了全新骨架的 de novo 小分子设计,刻意避开 MRTX1133 的已知骨架。经过 PAINS 过滤、PoseBusters 3D 有效性检查、关键残基(Asp12、Asp69)相互作用约束、Glide 重对接一致性验证和分子动力学模拟等层层筛选后,三个可合成候选物被推进到实验验证。通过 HTRF 竞争性结合实验(compete against一个已知占据同一口袋的参考配体),两个化合物展现出 IC₅₀ 分别为 24 µM 和 36 µM 的抑制活性。
值得注意的几个细节:其中活性最好的 KRAS G12D-compound-3 由于合成复杂性,实际上是以四种立体异构体的混合物形式合成的,这可能低估了其真实活力。两个活性化合物(compound-1 和 compound-3)与知名抑制剂 MRTX1133 的 Tanimoto 相似性仅为0.12和0.15,彼此之间的相似性也仅有0.25——这证明 AnewOmni 确实发现了全新的化学骨架。结构分析显示,compound-3 的四氢异喹啉(THIQ)核心的质子化N-甲基在功能上模拟了 MRTX1133 的C4-双环胺,维持了与Asp12的关键盐桥;酚羟基与Asp69形成了氢键,重现了 MRTX1133 中萘酚基团的相互作用模式。更重要的是,该设计还超越了对参考骨架的模仿:一个酰胺键连接的苯胺基团延伸到溶剂暴露区域,与 Glu62、His95 和 Asp92 形成了一组互补的三联相互作用,其中与Asp92的氢键在 MRTX1133 中是不存在的。
多肽设计。 生成的多肽经过简单的理化过滤后,进行了100 ns的分子动力学(MD)模拟,保留轨迹稳定的候选物,并用 MM/PBSA 估算结合自由能进行排序。最终合成并通过 HTRF 实验测试了50条多肽(30条线性 + 20条环肽)。
结果令人振奋。线性多肽中7/30在100 µM下产生了超过50%的抑制率,对应23%的命中率(IC₅₀ < 100 µM),最强者 IC₅₀ 达到 2.37 µM 和 6.91 µM。环肽则取得了更高的命中率——7/20达到 IC₅₀ < 100 µM,对应35%的成功率,最佳 IC₅₀ 为 11.40 µM 和 11.59 µM。特别值得关注的是,训练数据中完全不包含环肽,环肽设计的成功完全来自模型的可编程图提示能力和跨模态迁移学习所获得的设计原则。
纳米抗体设计。 团队构建了一套将 AnewOmni 与 AlphaFold3(AF3)交替迭代的流水线。首先从 SAbDab 数据库中筛选出 CDR 贡献了大部分结合接触的抗体和纳米抗体框架区(framework),以最小化框架区对结合的影响。随后交替进行 CDR 生成(AnewOmni)和复合物结构预测(AF3),基于表位覆盖率和 CDR 形成的相互作用比例进行排序。经过迭代后,来自三个框架(PDB ID: 8G70, 3JBE, 4W6X)的纳米抗体被富集出来,值得注意的是这三个框架在原始复合物中的靶标与 KRAS G12D 并无相似性。
实验验证采用了两种互补策略。第一种选择 AnewOmni 生成结构与 AF3 预测结构之间自一致性 RMSD(scRMSD)低于 5.0 Å 的设计——需要指出的是 AF3 倾向于预测其他表位而非研究者指定的表位,因此能通过这一筛选的设计本身就很少。在合成的四个候选中,三个纳米抗体通过 BLI 测定展现出单位数微摩尔亲和力,成功率达75% 。第二种更为激进的策略仅凭高生成似然排序,不强制结构自一致性。三个候选中一个展现了 Kd = 587 nM 的亚微摩尔结合亲和力——虽然成功率较低,但获得了比第一种策略更强的亲和力。
实验验证二:PCSK9的正构与变构双重抑制
心血管疾病每年在欧洲造成超过400万人死亡,占全部死亡人数的近47%,低密度脂蛋白(LDL)胆固醇升高是主要风险因素之一。前蛋白转化酶 subtilisin/kexin 9 型(PCSK9)是LDL代谢的关键调节因子。正常生理条件下,LDL经由LDLR结合后内吞并在溶酶体中降解,LDLR随后被回收到细胞表面继续工作。PCSK9 通过结合 LDLR 并稳定其构象,阻止 LDLR 回收,将 PCSK9–LDLR 复合物引向溶酶体降解,从而降低细胞表面的 LDLR 数量,间接导致血浆 LDL 胆固醇升高。
抑制 PCSK9–LDLR 的蛋白-蛋白相互作用(PPI)是增强 LDLR 回收、降低血浆 LDL 胆固醇的有力策略。然而这一 PPI 界面大且平坦,给分子设计带来了极大挑战。研究团队在此展示了 AnewOmni 的正构(orthosteric)多肽设计与变构(allosteric)小分子设计双管齐下的策略。
正构多肽。 团队设计了10到12个残基的线性多肽,靶向 PCSK9 的 PPI 界面。受到前述纳米抗体设计中基于似然排序的良好表现的鼓舞,这次完全采用无监督生成似然作为唯一筛选标准。共生成5,000个候选多肽,计算似然分布的均值(µ)和标准差(σ),以 µ + 3σ 为阈值选出7条似然特别高的多肽进行合成和实验测试。SPR 测定显示,7条多肽中4条结合了 PCSK9,Kd 低于 10 µM,对应 57%的命中率,最优者 Kd 达到 3.19 µM 和 4.02 µM。
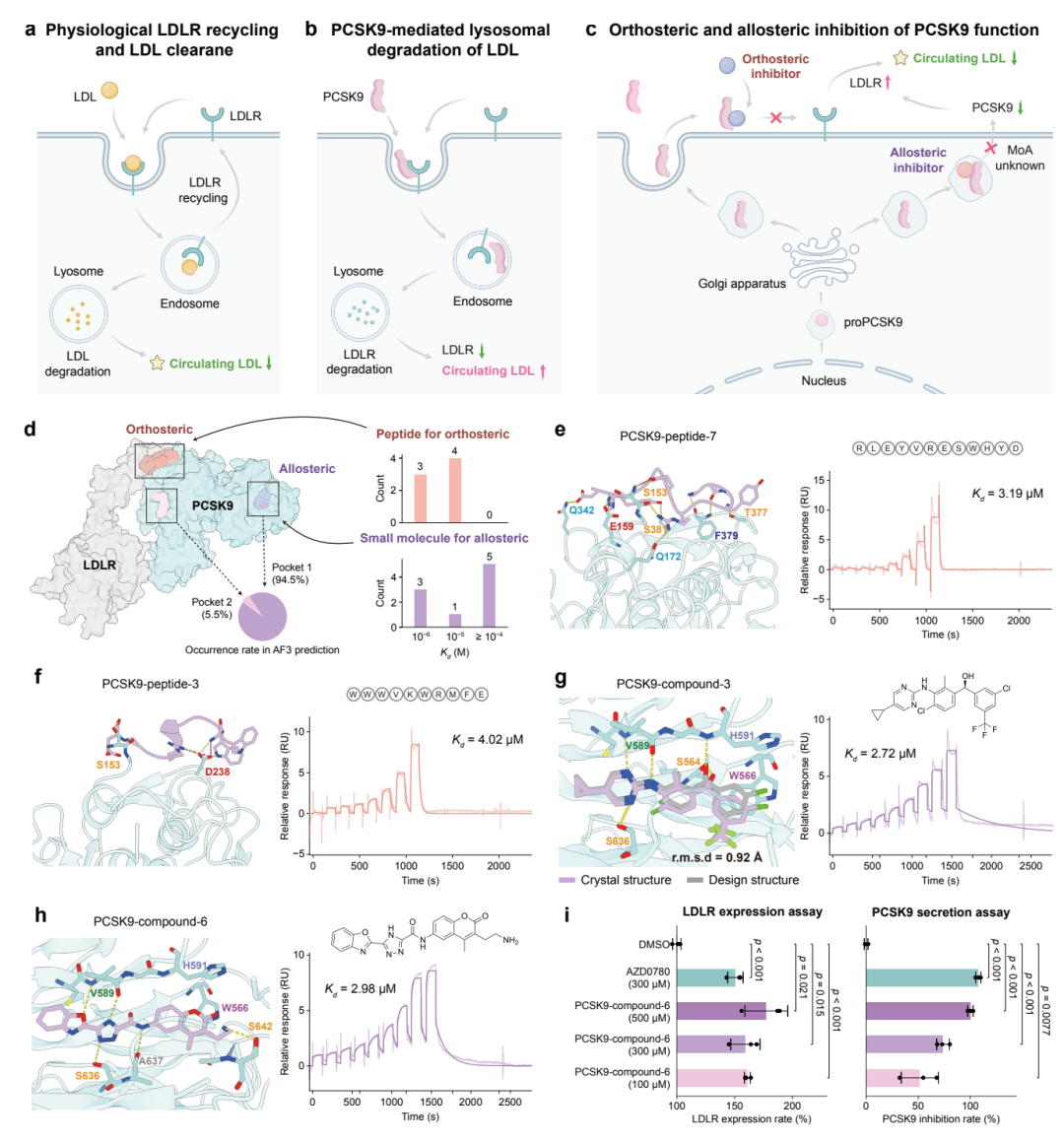
变构小分子。 这是整篇工作中最引人注目的部分之一。AZD0780 是最近报道的一种具有良好临床特征的 PCSK9 小分子调节剂,但它并不直接抑制 PCSK9–LDLR 相互作用,其精确的结合位点和作用机制至今不明。受到这一线索的启发,团队首先利用 AlphaFold3 预测了1,000个 PCSK9 与 AZD0780 的复合物结构。结果令人瞩目:94.5%的预测收敛于 PCSK9 C末端域(CTD)上的一个隐蔽结合位点。
以这个预测出的变构位点作为设计靶标,AnewOmni 生成候选小分子,经筛选后合成了9个设计用于实验评估。SPR 测定显示三个化合物结合了 PCSK9,Kd 低于 10 µM,最优者(PCSK9-compound-3 和 PCSK9-compound-6)分别达到 Kd = 2.72 µM 和 2.98 µM。
功能层面的验证同样令人兴奋。细胞实验测定 LDLR 表达水平后发现,PCSK9-compound-6 在 100 µM 浓度下即可达到与 AZD0780 在 300 µM 浓度下相当的 LDLR 上调效果。鉴于该变构位点位于与 PCSK9 分泌相关的 CTD 上,团队进一步评估了化合物对 PCSK9 分泌的影响——细胞实验表明 AZD0780 和 PCSK9-compound-6 均能有效抑制 PCSK9 分泌,提示了一种可能的作用机制:变构结合通过干扰 PCSK9 分泌来减少 PCSK9 介导的 LDLR 降解。
最具说服力的证据来自晶体学。团队以 2.70 Å 分辨率解析了 PCSK9-compound-3 与 PCSK9 的共晶结构。结构叠合显示,该化合物恰好占据了预测的变构口袋,且 AnewOmni 生成的结合构象与实验确定的构象之间的 RMSD 仅为 0.92 Å。这一结果有力地证明了模型在原子分辨率下设计分子结合物的结构精度。
局限性与未来展望
尽管成果令人瞩目,论文也坦诚讨论了当前流程的几项局限。首先,基于 AlphaFold3 预测或物理模拟的后筛选步骤计算开销仍然较大。虽然初步结果显示模型自身的无监督似然有可能作为轻量级替代品部分绕过这些筛选,但其跨靶标、跨模态的普适性仍需更广泛的验证。其次,当前框架尚不能显式控制结合亲和力——虽然生成流程能有效产出阳性结合物,但没有计算指标能够指示单个设计的亲和力水平。
不过,论文在讨论部分也描绘了令人期待的方向。可编程图提示机制使得化学、拓扑和几何的精细控制不再依赖重新训练,满足了多样化下游应用的复杂定制需求。跨模态迁移进一步暗示了在模态之间进行模拟的可能——例如将抗体转化为多肽以获得细胞穿透性,同时保留关键的相互作用模式。更广泛地看,AnewOmni 预示着未来的分子设计系统将超越模态特异性流水线,走向更通用的分子推理引擎,有望将分子设计推进到数据和人类直觉都极为有限的化学空间中。
写在最后
回顾整篇工作,AnewOmni 的核心贡献可以归结为三个层次的首次:首次证明跨模态联合训练在适当的表示粒度下可以带来互惠性能增益和训练分布外的泛化改善;首次在统一框架内实现了从小化学实体到大型生物制剂的跨尺度实验验证;首次通过晶体结构确认了生成模型在原子分辨率下的结合模式预测精度(RMSD 0.92 Å)。
在 AlphaFold3、RFDiffusion、Boltz-2等重磅工作层出不穷的今天,这篇工作走出了一条独特的路径——不是预测结构,而是生成结构;不是单一模态,而是统一所有模态。最终,它所指向的方向或许是AI药物设计的终极形态:一个真正理解分子识别底层物理化学原理的通用生成引擎,能够自如地在不同分子模态之间迁移设计知识,并在人类化学直觉尚未涉足的空间中开辟新路。
论文信息
Programming Biomolecular Interactions with All-Atom Generative Model
Xiangzhe Kong, Junwei Chen, Ziting Zhang, Gaodeng Li 等
bioRxiv, 2026年3月15日
DOI: https://doi.org/10.64898/2026.03.12.711044
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-03-17,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

