Cell | 生成式AI如何攻克癌症复杂性难题
Cell | 生成式AI如何攻克癌症复杂性难题

DrugAI
发布于 2026-04-28 10:16:50
发布于 2026-04-28 10:16:50
DRUGONE
癌症“标志性特征(Hallmarks of Cancer)”框架在推动人类理解癌症生物学方面发挥了奠基性作用。该框架通过将癌症抽象为一组共通的功能能力,实现了对复杂现象的统一解释。然而,这种方法本质上是一种简化建模,虽能揭示关键机制,却难以解释不同尺度之间的相互作用。
因此,亟需新的方法来刻画癌症所固有的复杂性、多模态性以及多尺度特征。研究人员提出,基于人工智能最新进展构建的生成式模型,有望成为应对这一挑战的关键技术。这类模型能够识别复杂模式、处理非结构化信息并整合多模态数据,从而在癌症的诊断、理解和干预方面带来变革。
最终,研究人员设想形成一种协同体系:生成式模型驱动假设生成与科学发现,而癌症标志性框架则指导实验设计与测量工具的发展,两者相互促进,共同推动癌症研究进入新阶段。

癌症是一种高度复杂且异质的疾病。经典的“癌症标志性特征”框架通过提出一系列基本原则,帮助研究人员系统理解正常细胞如何转化为恶性细胞,并进一步发展为肿瘤。这些原则基于细胞生物学的基本规律,即细胞增殖、分化与死亡由一套保守的分子机制所控制。
尽管该框架在统一癌症研究方面取得巨大成功,但其本质上的“简化性”也带来了局限。它难以完整描述癌症在分子、细胞、组织乃至个体层面的复杂互动关系,也难以直接转化为精准的临床干预策略。
过去几十年中,癌症治疗取得显著进展,五年生存率大幅提升。然而,这一进步正在趋于平台期,传统方法在推动进一步突破方面面临瓶颈。因此,研究人员认为,需要引入新的技术范式,从系统层面重新建模癌症。
生成式模型正是在这一背景下被提出。与传统针对单一任务的AI不同,这类模型能够直接从真实世界数据中学习复杂分布,并将癌症视为一种动态演化的系统现象,从而为理解和干预提供全新路径。
从检测到干预:AI在癌症中的扩展角色
癌症检测
人工智能在癌症领域最成熟的应用集中在检测阶段。医学影像(如CT、MRI、病理切片)与分子检测技术为AI提供了丰富的数据基础。深度学习的发展使AI能够在图像识别任务中达到甚至超越人类水平,从而推动了癌症检测性能的显著提升。
例如,AI已成功应用于皮肤癌识别、乳腺癌筛查、肺癌检测及病理图像分析等多个领域。这些方法不仅提高了诊断准确率,还推动了临床级AI产品的诞生。
近年来,基于Transformer和自监督学习的“基础模型”进一步提升了模型泛化能力,使得同一模型可以适用于多种下游任务。此外,多模态学习(如图像+文本、图像+分子数据)也逐渐成为趋势,为更全面的诊断提供支持。
与此同时,AI不仅能识别已知特征,还开始挖掘新的生物学信息。例如,通过常规病理图像预测基因突变、治疗反应或预后等,显示出AI在隐含信息提取方面的潜力。
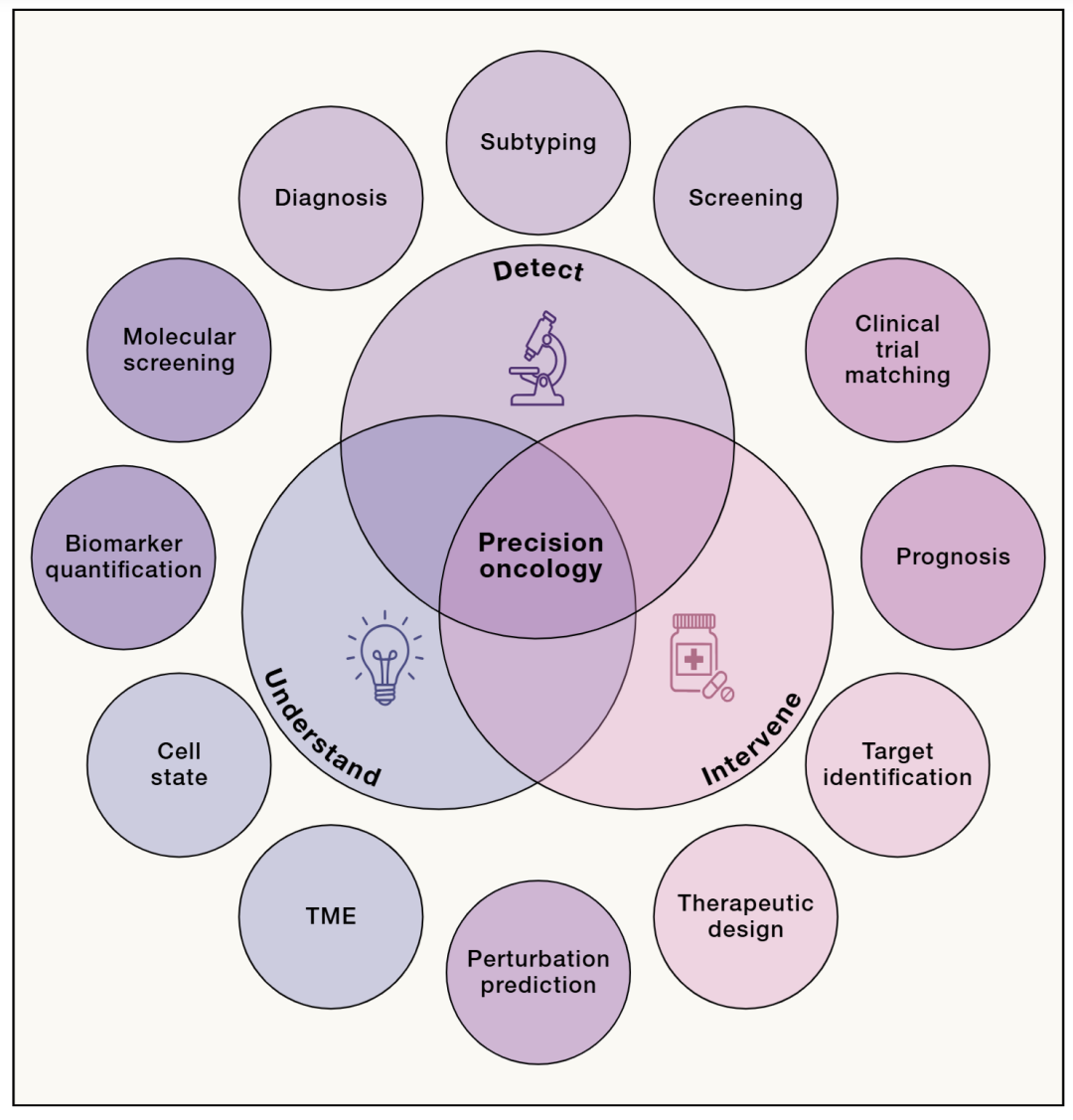
图1:AI在癌症检测、理解与干预中的应用框架。
癌症理解
在癌症生物学研究中,分子层面的测量(如基因组、转录组、蛋白组)提供了重要信息。然而,仅依赖基因突变信息已难以解释治疗反应和耐药性。
研究人员逐渐将重点转向“细胞状态”,即通过转录组数据刻画细胞在特定时间点的动态功能状态。单细胞RNA测序与空间转录组技术的兴起,使研究人员能够更精细地解析肿瘤内部异质性。
AI在这一领域的作用主要体现在处理高维、噪声数据并构建基础模型。例如,单细胞模型可用于细胞类型识别、扰动响应预测等任务。但当前模型仍存在数据构建、泛化能力和评估体系等方面的挑战。
多模态整合被认为是未来的重要方向。将转录组数据与病理图像结合,有望在细胞与组织层面同时获得新的生物学洞察。
癌症干预
在治疗层面,AI正逐步参与到临床决策中。例如,通过整合多模态数据预测治疗响应、匹配临床试验或优化患者分层。
已有研究表明,AI可以显著提高早期检测率、优化治疗选择,并改善患者预后。例如在乳腺癌筛查中,AI可提升超过20%的检测率;在免疫治疗中,多模态模型优于传统生物标志物。
然而,AI在临床应用中仍面临挑战,包括模型验证、流程整合以及公平性问题。当前阶段,AI更适合作为辅助决策工具,而非完全自动化系统。
用生成式模型应对癌症复杂性
传统科学建模通常通过简化系统来获得可解释性,而生成式模型则采取相反策略:直接学习复杂性本身。
研究人员认为,生成式模型可以作为“癌症标志性特征”的重要补充工具。它们具备三大核心能力:
复杂模式识别
生成式模型能够从海量数据中学习人类难以描述的复杂模式。例如,在图像识别、蛋白质结构预测和语言生成等领域,这类模型已展现出超越人类的能力。
在癌症研究中,这意味着模型可以从多模态数据中发现隐藏规律,从而揭示新的生物学机制。
多模态融合
癌症涉及多个层级,从分子到组织再到临床表现。生成式模型能够整合不同模态的数据,例如影像、基因组、转录组和临床信息,从而形成统一表示。
这种能力使其可以在体外模拟实验、预测药物效果,并优化实验设计。
非结构化输入与上下文学习
生成式模型能够处理非结构化数据,并通过上下文学习整合新信息。例如,模型可以结合患者病理图像与实验筛选结果,动态调整治疗建议。
这种能力使模型能够在实际应用中不断更新知识,而无需重新训练。
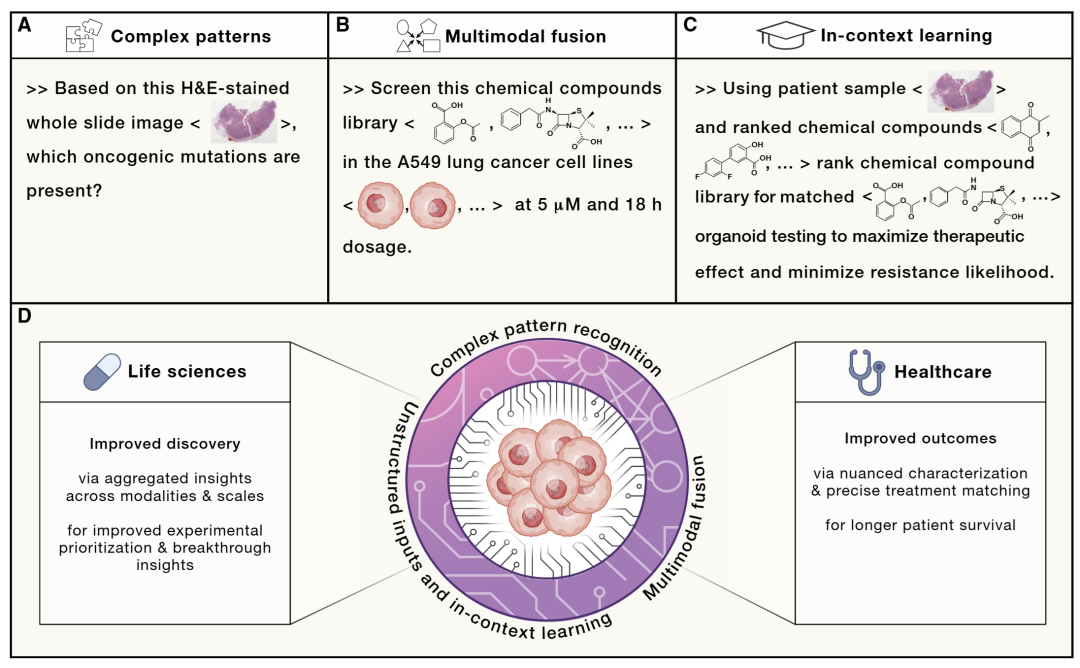
图2:生成式模型能力及其在癌症研究与医疗中的应用。
通过行动学习:癌症研究的新范式
生成式模型引入了一种全新的科学研究模式。与传统逐步解析机制不同,这类模型可以在大规模假设空间中快速筛选潜在答案。
尽管其可解释性较弱,但研究人员可以通过实验验证模型提出的假设,从而实现“数据—模型—实验”的闭环。
这种闭环机制将带来新的科学发现路径:模型提出假设,实验验证结果,反馈再用于优化模型。长期来看,这一过程将形成持续进化的研究体系,加速癌症理解与治疗发展。
结论与展望
癌症标志性特征框架为理解癌症提供了基础,但其简化性限制了对复杂系统的全面刻画。生成式模型则提供了一种新的建模范式,通过整合多模态数据与上下文信息,构建更加动态和全面的癌症表示。
未来,生成式模型有望在体内模拟实验、机制发现及精准医疗中发挥关键作用。同时,其成功应用仍依赖于临床验证、伦理规范及基础设施建设。
研究人员认为,癌症研究正进入一个新的阶段:从静态、分离的分析转向动态、系统化建模。在这一过程中,生成式模型将成为连接数据、机制与临床实践的核心桥梁。
整理 | DrugOne团队
参考资料
Conard, A.M., Hughes, M., Hall, J., Tenenholtz, N., Zimmermann, E., Crawford, L., Amini, A.P. and Severson, K., 2026. Tackling the complexity of cancer with generative models. Cell, 189(8), pp.2218-2231.
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-20,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

