ACES-GNN:赋能图神经网络解析药物发现中的活性悬崖机制
ACES-GNN:赋能图神经网络解析药物发现中的活性悬崖机制

MindDance
发布于 2026-01-08 13:04:58
发布于 2026-01-08 13:04:58
ACES-GNN: can graph neural network learn to explain activity cliffs?
期刊: Digital Discovery 链接: https://doi.org/10.1039/d5dd00012b 代码: https://github.com/Liu-group/XACs https://doi.org/10.5281/zenodo.15558394 简介: 该论文针对图神经网络(GNN)在药物发现中存在的 “黑箱” 问题,提出了活性悬崖解释监督图神经网络(ACES-GNN)框架,其创新点在于将活性悬崖(ACs)的解释监督融入 GNN 训练,同时提升预测精度与可解释性。该方法通过构建包含非共有亚结构损失和共有亚结构损失的复合目标函数,引导模型关注导致活性差异的关键亚结构。实验在涵盖 30 个药理学靶点的数据集(含 48707 个分子)上进行,结果显示 ACES-GNN 在 28 个靶点上提升了解释性,18 个靶点同时提升了预测性与解释性,且预测与解释性能存在正相关。该论文证明了解释引导学习在分子建模和药物发现中的潜力,为可解释人工智能的发展提供了有效框架。

在分子性质预测领域,图神经网络(GNNs)凭借其对分子图结构的卓越建模能力,已成为定量构效关系(QSAR)研究的核心工具。然而,其"黑箱"特性所导致的决策不透明性,严重制约了在药物发现等对解释性要求严苛的领域中的应用。特别是面对活性悬崖(ACs)这一关键挑战——即结构相似分子呈现显著活性差异的现象时,传统模型往往因过度依赖共享结构特征而表现不佳。近期发表于《Digital Discovery》的研究"ACES-GNN: can graph neural network learn to explain activity cliffs?"提出了一种创新性的解决方案,通过构建活性悬崖解释监督框架,实现了预测精度与可解释性的协同提升,为可解释人工智能在分子建模中的应用开辟了新路径。
活性悬崖解析的核心挑战与现有局限
活性悬崖的准确定义和有效解析是药物研发中的关键科学问题。研究中采用的ACs定义为:分子对结构相似度(基于亚结构、骨架或SMILES字符串)超过90%,且生物活性差异达到10倍以上(|ΔpKi|>1.0或|ΔpEC50|>1.0)。这类特殊分子对的存在揭示了一个核心规律:微小的结构修饰可能引发生物活性的剧烈变化,而识别这些关键修饰位点,对药物分子优化具有直接指导意义。
现有GNN模型在处理ACs时面临双重困境。一方面,预测性能上存在"脚手架内泛化"问题,即模型难以对结构高度相似的分子做出差异化预测;另一方面,解释性上,主流的可解释人工智能(XAI)方法多移植自其他领域,应用于分子解释时常常产生化学意义不明的归因结果。例如,基于扰动的GNNExplainer可能高亮不构成化学功能片段的节点或边,无法满足 medicinal chemists 对结构化解释的需求。更关键的是,这些方法仅能事后解释模型输出,无法改变模型内部决策逻辑,因此难以避免"Clever Hans"效应——即模型通过虚假关联做出正确预测,却无法提供可靠的科学依据。
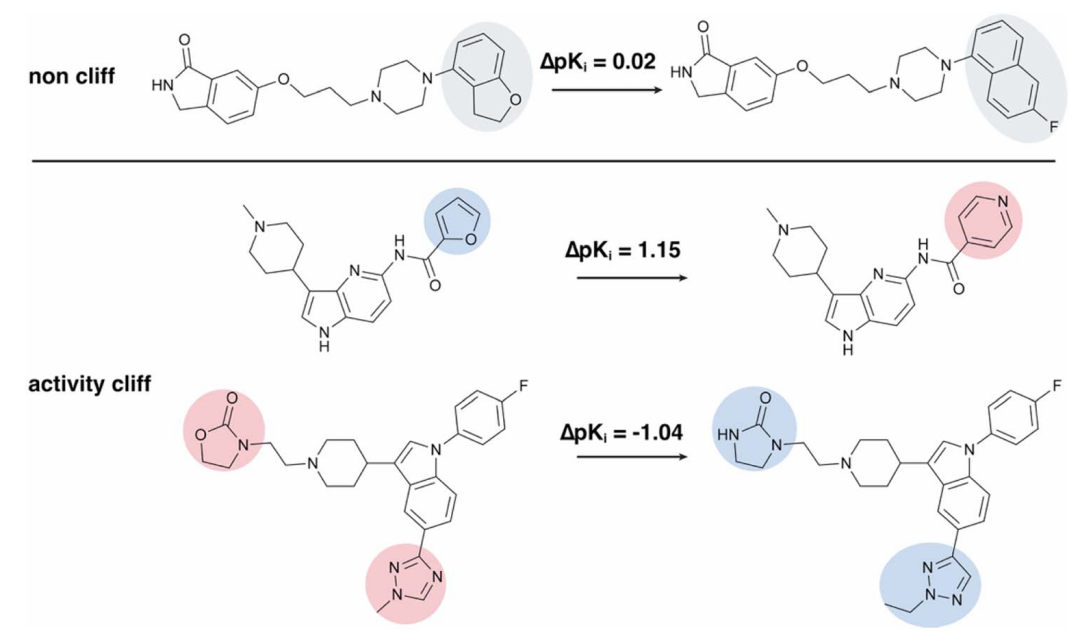
该图展示了来自 CHEMBL214 数据集的分子对示例,直观区分了非悬崖和活性悬崖(AC)分子对。对于结构高度相似的分子对,图中高亮了它们的差异亚结构:非悬崖分子对(|ΔpKi|<1.0)的差异亚结构以灰色标注;活性悬崖分子对(|ΔpKi|>1.0)中,差异亚结构若降低 pKi 则标为红色,若升高 pKi 则标为蓝色。此图清晰呈现了活性悬崖的核心特征 —— 微小结构差异导致显著活性变化,为后续解释监督的设计提供了直观依据。
该图展示了来自 CHEMBL214 数据集的分子对示例,直观区分了非悬崖和活性悬崖(AC)分子对。对于结构高度相似的分子对,图中高亮了它们的差异亚结构:非悬崖分子对(|ΔpKi|<1.0)的差异亚结构以灰色标注;活性悬崖分子对(|ΔpKi|>1.0)中,差异亚结构若降低 pKi 则标为红色,若升高 pKi 则标为蓝色。此图清晰呈现了活性悬崖的核心特征 —— 微小结构差异导致显著活性变化,为后续解释监督的设计提供了直观依据。
ACES-GNN框架的创新设计与理论基础
ACES-GNN(Activity-Cliff-Explanation-Supervised GNN)框架的核心突破在于,将活性悬崖的解释监督直接嵌入GNN训练过程,使模型在学习预测分子活性的同时,主动习得符合化学直觉的解释逻辑。这一设计基于两个关键假设:其一,模型对AC分子对中非共有亚结构的归因,应能反映活性差异的方向;其二,应减少对共有结构的过度关注,避免因共享特征偏见导致预测偏差。
为实现上述目标,研究构建了包含预测损失和解释损失的复合目标函数。预测损失采用均方误差(MSE),衡量模型对pKi或pEC50值的预测精度;解释损失则由两部分构成:非共有亚结构损失()和共有亚结构损失()。其中,非共有亚结构损失通过成对排序约束,确保非共有原子集的归因总和与活性差异方向一致,数学表达为;共有亚结构损失则通过L2正则化最小化共有原子集的归因强度,公式为。总损失函数为,其中λ为平衡参数,通过网格搜索优化。
这种设计的精妙之处在于,它将化学领域对ACs的认知(非共有亚结构是活性差异的关键驱动因素)转化为可量化的数学约束,迫使模型学习既具有预测能力又符合领域知识的分子表征。与事后解释方法相比,ACES-GNN从根本上改变了模型的学习目标,使解释性成为模型内在属性而非附加功能。
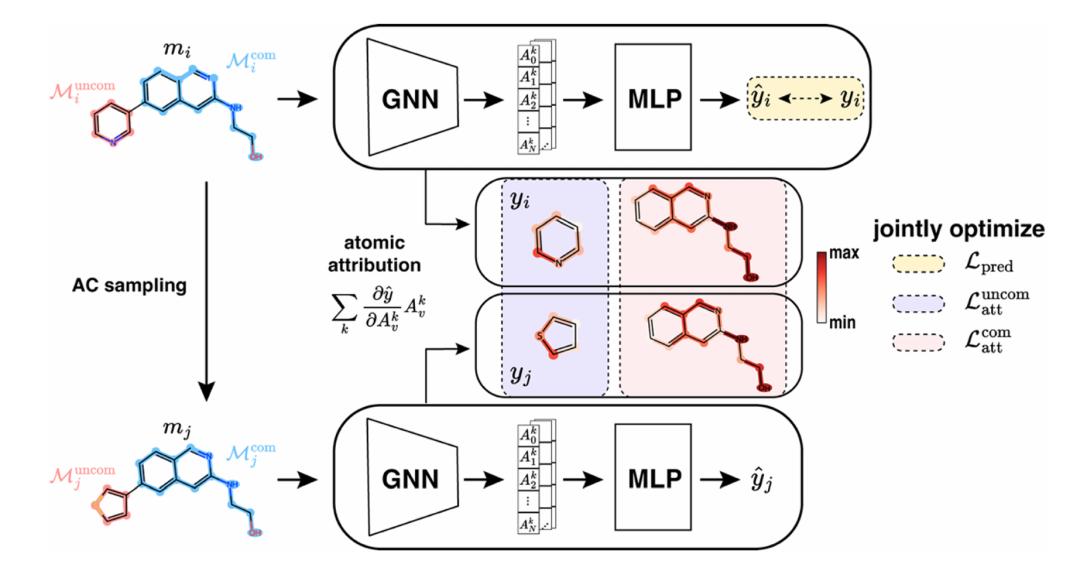
该图展示了 ACES-GNN 的训练流程。对于无 AC 对的分子,模型遵循标准 GNN 训练流程,仅优化预测损失);对于有 AC 对的分子,从训练集中采样其 AC 配对分子,计算梯度归因,并与 ground-truth 解释对比,引入归因损失(包括非共有亚结构损失和共有亚结构损失))。总损失结合预测损失和归因损失,实现预测精度与解释性的联合优化,体现了框架将解释监督融入训练的核心设计。
该图展示了 ACES-GNN 的训练流程。对于无 AC 对的分子,模型遵循标准 GNN 训练流程,仅优化预测损失);对于有 AC 对的分子,从训练集中采样其 AC 配对分子,计算梯度归因,并与 ground-truth 解释对比,引入归因损失(包括非共有亚结构损失和共有亚结构损失))。总损失结合预测损失和归因损失,实现预测精度与解释性的联合优化,体现了框架将解释监督融入训练的核心设计。
多维度实验验证与性能分析
研究在包含30个药理学靶点的基准数据集上系统评估了ACES-GNN的性能,该数据集源自ChEMBLv29,涵盖激酶、核受体、转移酶和蛋白酶等多个家族,包含48707个有机分子(35632个独特分子),单个靶点数据集规模在600至3700个分子之间,具有广泛的代表性。实验设计采用基于ECFP的谱聚类分层抽样,将数据集按8:1:1划分为训练集、验证集和测试集,并对每个靶点进行10次重复实验以确保结果稳健性。
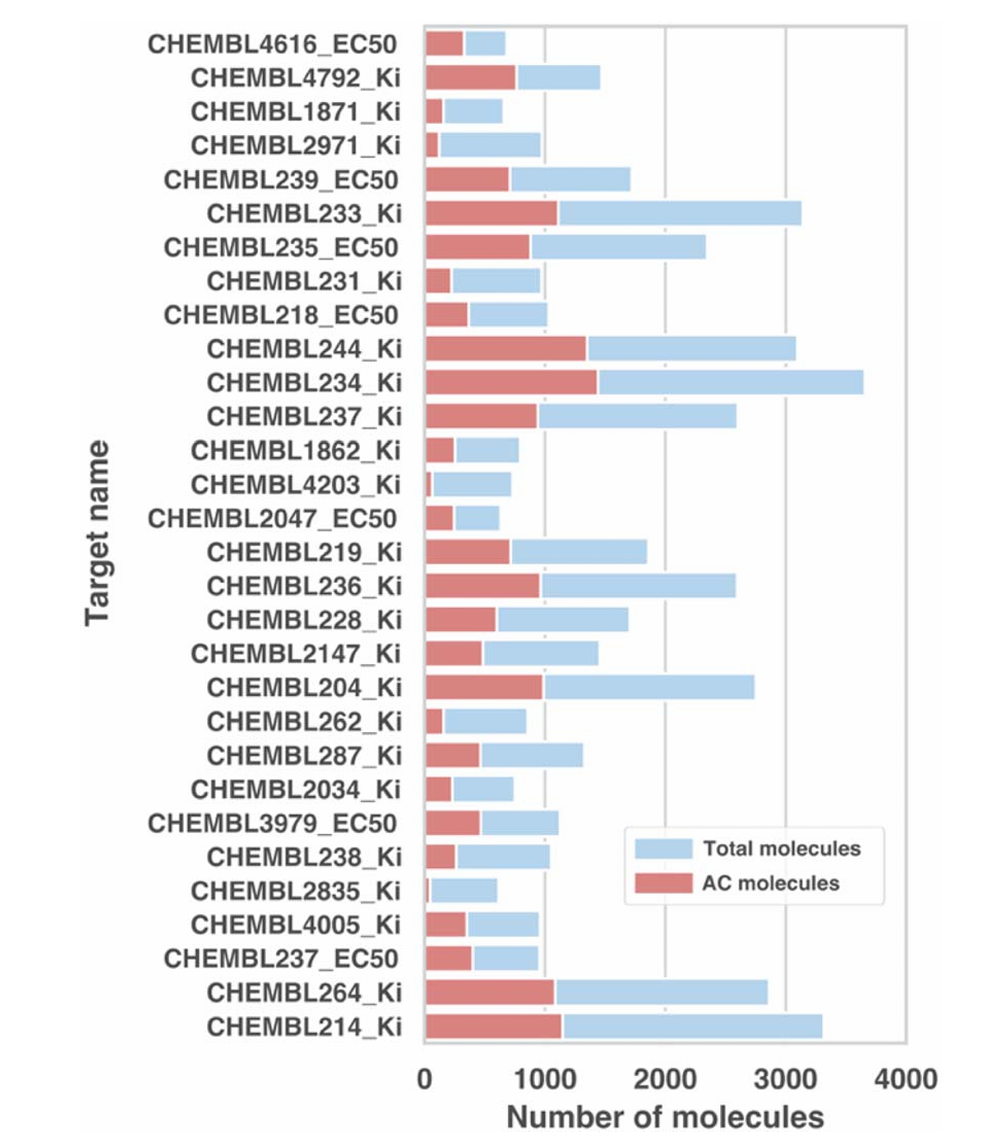
该图展示了 30 个靶点数据集的分子数量分布,包括每个靶点的总分子数和活性悬崖(AC)分子数,数据集名称后缀标注了 potency 指标(Ki 或 EC50)。结果显示,AC 分子占比在 8% 到 52% 之间,多数靶点约含 30% 的 AC 分子,数据集规模从 600 到 3700 个分子不等,反映了药物发现中分子集合的典型规模和多样性,为模型验证提供了全面的测试场景。
该图展示了 30 个靶点数据集的分子数量分布,包括每个靶点的总分子数和活性悬崖(AC)分子数,数据集名称后缀标注了 potency 指标(Ki 或 EC50)。结果显示,AC 分子占比在 8% 到 52% 之间,多数靶点约含 30% 的 AC 分子,数据集规模从 600 到 3700 个分子不等,反映了药物发现中分子集合的典型规模和多样性,为模型验证提供了全面的测试场景。
在解释性能方面,以"全局方向"指标(正确归因占比)衡量,ACES-MPNN结合GradCAM的方法在30个靶点中的28个表现优于无监督GNN,其中18个靶点的提升具有统计显著性(p<0.05)。与其他梯度归因方法(GradInput、SmoothGrad、IG)相比,ACES框架下的GradCAM归因与化学直觉的一致性最高,平均全局方向得分达到0.765,显著高于未监督的0.722。这一结果验证了解释监督能够有效引导模型关注化学意义显著的亚结构。
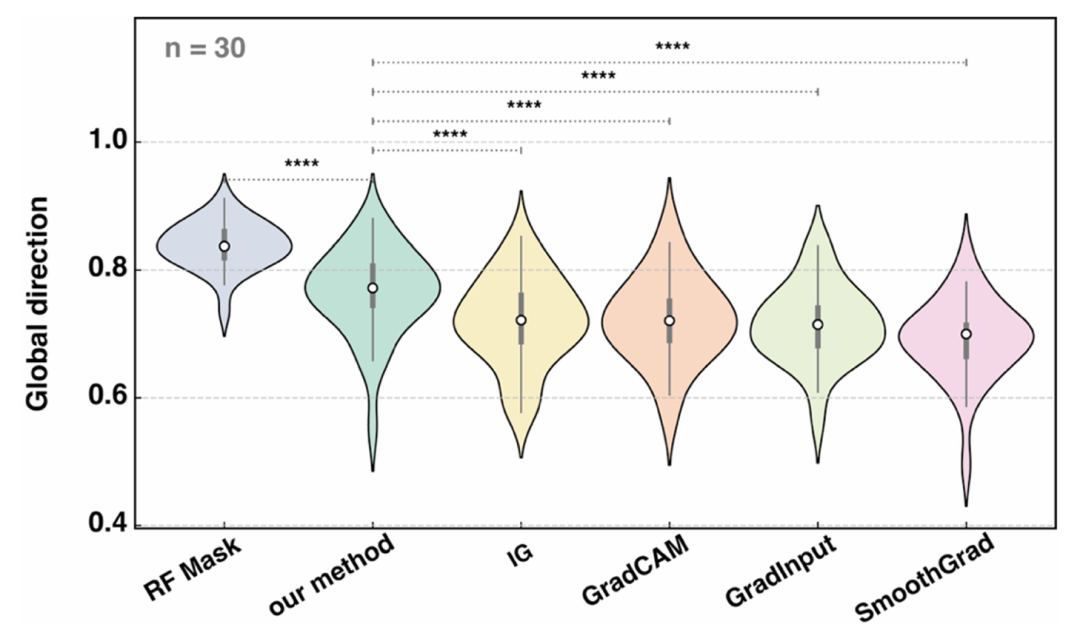
该图以 “全局方向” 指标(越高表示解释性越好)对比了 ACES-MPNN(结合 GradCAM)与其他方法的解释性能,包括无监督 GNN 结合多种梯度归因方法(GradCAM、GradInput 等)及随机森林(RF)结合 ECFP 的扰动掩码法。结果显示,ACES-MPNN 的全局方向得分显著高于其他梯度归因方法(p<0.0001),虽略低于 RF+ECFP,但验证了解释监督能有效提升 GNN 的解释质量,且梯度方法更具计算效率。
该图以 “全局方向” 指标(越高表示解释性越好)对比了 ACES-MPNN(结合 GradCAM)与其他方法的解释性能,包括无监督 GNN 结合多种梯度归因方法(GradCAM、GradInput 等)及随机森林(RF)结合 ECFP 的扰动掩码法。结果显示,ACES-MPNN 的全局方向得分显著高于其他梯度归因方法(p<0.0001),虽略低于 RF+ECFP,但验证了解释监督能有效提升 GNN 的解释质量,且梯度方法更具计算效率。
预测性能评估显示,ACES-GNN在AC分子的预测上表现尤为突出。对于MPNN骨干网络,ACs分子的RMSE(RMSE_cliff)从0.829降至0.814,降低1.8%;GIN和GAT骨干网络的RMSE_cliff分别降低8.9%和6.3%,且这种改进在统计上具有显著性(p<0.01)。值得注意的是,RMSE的改善主要源于对极端误差的控制,而MAE指标变化不显著,表明解释监督特别有助于减少AC预测中的大幅偏差,这与药物发现中对预测可靠性的实际需求高度契合。
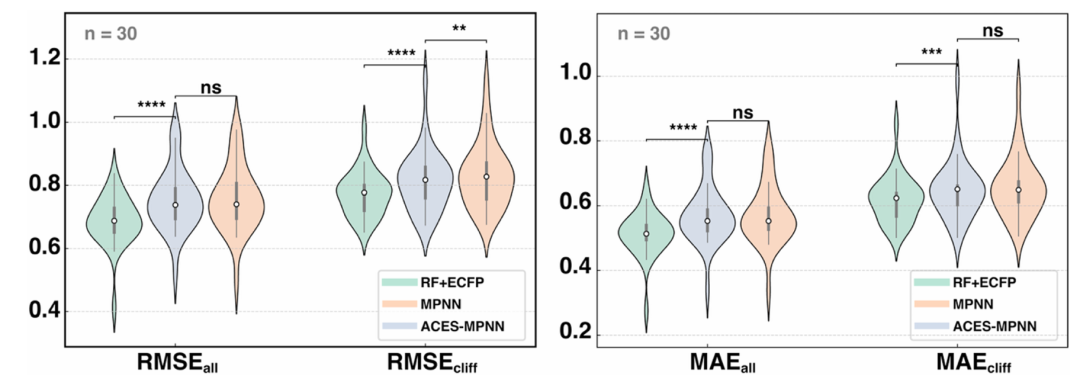
该图通过小提琴图对比了 ACES-MPNN、无监督 MPNN 和 RF+ECFP 在 30 个靶点上的预测性能,指标包括全数据集的 RMSE(RMSE_all)、AC 分子的 RMSE(RMSE_cliff)及对应的 MAE。结果显示,ACES-MPNN 的 RMSE_cliff 显著低于无监督 MPNN(p<0.01),说明解释监督能有效减少 AC 分子的预测误差,尤其降低了 RMSE 敏感的极端误差,但 MAE 提升不显著,体现了其在缓解活性悬崖预测难题上的针对性优势。
该图通过小提琴图对比了 ACES-MPNN、无监督 MPNN 和 RF+ECFP 在 30 个靶点上的预测性能,指标包括全数据集的 RMSE(RMSE_all)、AC 分子的 RMSE(RMSE_cliff)及对应的 MAE。结果显示,ACES-MPNN 的 RMSE_cliff 显著低于无监督 MPNN(p<0.01),说明解释监督能有效减少 AC 分子的预测误差,尤其降低了 RMSE 敏感的极端误差,但 MAE 提升不显著,体现了其在缓解活性悬崖预测难题上的针对性优势。
消融实验进一步揭示了复合损失函数中各组件的作用:单独使用非共有亚结构损失或共有亚结构损失均能带来性能提升,但两者结合时效果最优。其中,非共有亚结构损失对全局方向得分的提升贡献更大(与该指标的定义直接相关),而共有亚结构损失则在减少模型对冗余共享特征的依赖方面发挥关键作用。
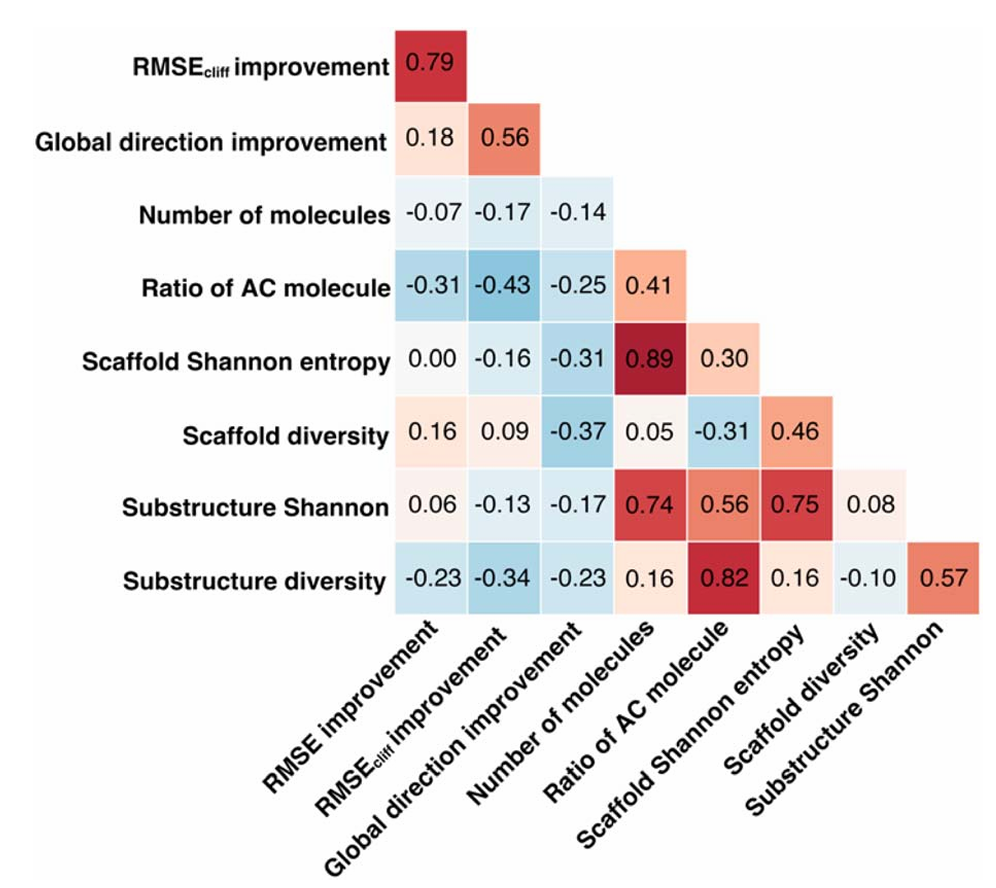
该图展示了模型性能改进(RMSE、RMSE_cliff、全局方向得分)与数据集特征(分子数、AC 比例、骨架多样性等)的 Pearson 相关系数。结果显示,RMSE_cliff 改进与全局方向改进呈强正相关(0.56),验证了解释性提升与预测性能优化的一致性;同时,AC 比例和亚结构多样性与性能改进呈负相关,表明解释监督在 AC 比例低、亚结构多样性低的数据集上效果更显著。
该图展示了模型性能改进(RMSE、RMSE_cliff、全局方向得分)与数据集特征(分子数、AC 比例、骨架多样性等)的 Pearson 相关系数。结果显示,RMSE_cliff 改进与全局方向改进呈强正相关(0.56),验证了解释性提升与预测性能优化的一致性;同时,AC 比例和亚结构多样性与性能改进呈负相关,表明解释监督在 AC 比例低、亚结构多样性低的数据集上效果更显著。
分子表征优化与机制分析
为深入理解ACES-GNN性能提升的内在机制,研究通过Representation-Property-Similarity Map(RPSMap)可视化分子表征空间。结果显示,ECFP表征主要分布在RPSMap的I区和III区,ACs问题不显著;而未监督MPNN的表征则聚集在高相似区域(右侧),即使分子活性差异显著也难以区分,表现出对ACs的固有敏感性。相比之下,ACES-MPNN的表征空间中,原本位于IV区(高相似-高活性差异,即ACs)的分子对明显向III区(低相似-高活性差异)转移,表明解释监督使模型能够更好地捕捉导致活性差异的结构特征,从而优化了表征-性质关系。
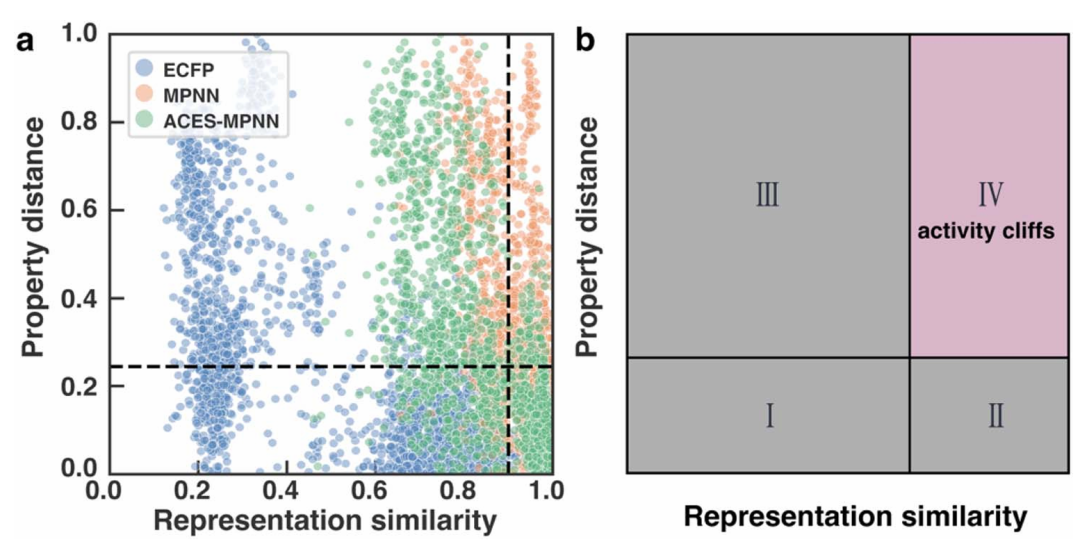
该图通过表征 - 性质 - 相似度映射(RPSMap)对比了 ECFP、无监督 MPNN 和 ACES-MPNN 的分子表征质量,以 CHEMBL2835 测试集为例。图中 y 轴为归一化性质距离,x 轴为表征相似度,活性悬崖(AC)位于高相似度 - 高性质距离的 IV 区。结果显示,ACES-MPNN 能将 IV 区的 AC 分子对向 III 区(低相似度 - 高性质距离)转移,表明其优化了表征空间,使结构相似但活性不同的分子具有更具区分度的表征,解释了预测性能提升的原因。
该图通过表征 - 性质 - 相似度映射(RPSMap)对比了 ECFP、无监督 MPNN 和 ACES-MPNN 的分子表征质量,以 CHEMBL2835 测试集为例。图中 y 轴为归一化性质距离,x 轴为表征相似度,活性悬崖(AC)位于高相似度 - 高性质距离的 IV 区。结果显示,ACES-MPNN 能将 IV 区的 AC 分子对向 III 区(低相似度 - 高性质距离)转移,表明其优化了表征空间,使结构相似但活性不同的分子具有更具区分度的表征,解释了预测性能提升的原因。
进一步的相关性分析揭示了影响ACES框架效果的关键因素:RMSE_cliff改善与全局方向得分提升之间存在显著正相关(Pearson系数0.56,p=0.001),表明解释性提升与预测性能优化具有内在一致性,验证了"更好的解释带来更好的预测"这一核心假设。同时发现,AC分子比例高的数据集和亚结构多样性高的数据集,其RMSE_cliff改善较小,可能是由于高AC比例引入了更多噪声监督信号,而高度多样的亚结构增加了学习难度。这些发现为后续研究中数据集选择和方法优化提供了重要参考。
案例研究直观展示了ACES-GNN的解释优势:在CHEMBL239(过氧化物酶体增殖物激活受体α)、CHEMBL2835(Janus激酶1)和CHEMBL219(多巴胺D4受体)的AC分子对中,未监督MPNN的GradCAM归因要么未能区分关键亚结构,要么错误判断贡献方向;而ACES-MPNN的归因则准确高亮了导致活性差异的非共有亚结构,且贡献方向与实验结果一致。这种精准的局部解释能力,使其能够为化合物优化提供明确的结构修饰指导。
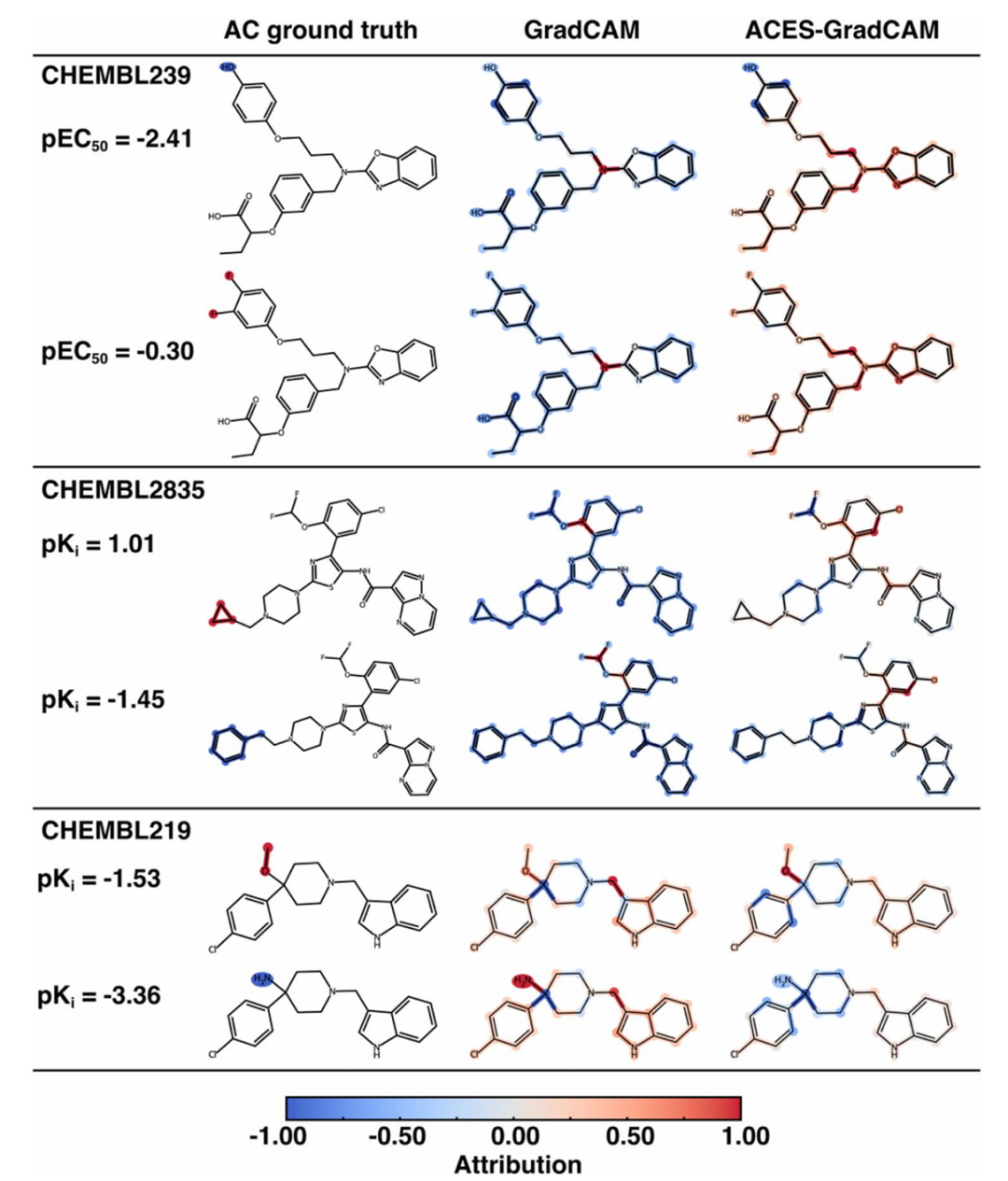
该图展示了 3 个靶点(CHEMBL239、CHEMBL2835、CHEMBL219)的 AC 分子对解释案例,对比了 ground-truth 标注、无监督 MPNN 的 GradCAM 归因和 ACES-MPNN 的 GradCAM 归因。结果显示,ACES-MPNN 的归因更精准:高亮了与活性差异相关的非共有亚结构,且归因方向与 ground-truth 一致;而无监督 MPNN 要么忽略关键差异亚结构,要么归因方向错误,直观验证了 ACES 框架在提升单个分子解释质量上的效果。
该图展示了 3 个靶点(CHEMBL239、CHEMBL2835、CHEMBL219)的 AC 分子对解释案例,对比了 ground-truth 标注、无监督 MPNN 的 GradCAM 归因和 ACES-MPNN 的 GradCAM 归因。结果显示,ACES-MPNN 的归因更精准:高亮了与活性差异相关的非共有亚结构,且归因方向与 ground-truth 一致;而无监督 MPNN 要么忽略关键差异亚结构,要么归因方向错误,直观验证了 ACES 框架在提升单个分子解释质量上的效果。
结论与展望
ACES-GNN框架通过将活性悬崖解释监督融入GNN训练,成功解决了传统模型在ACs预测与解释中的双重困境,在30个药理学靶点数据集上实现了预测精度与可解释性的协同提升。其核心贡献在于:提出了一种将化学领域知识(ACs的结构-活性关系)转化为可量化监督信号的有效方法;验证了解释性与预测性能之间的正相关性;展示了框架对不同GNN骨干网络的普适性。
该研究为药物发现中的可解释人工智能研究提供了重要启示:梯度归因方法能够有效整合领域先验知识;即使缺乏精确的物理基或人工标注解释,基于ACs的启发式解释也能显著提升模型泛化能力。未来研究可从三方面拓展:探索更先进的梯度归因技术(如预期梯度)以减少潜在偏差;开发因果亚结构识别方法以优化ACs的 ground-truth 定义;整合分子三维结构信息以进一步提升模型性能。
ACES-GNN不仅是技术上的创新,更代表了一种研究范式的转变——在科学发现领域,机器学习模型的解释性不应被视为附加要求,而应作为设计目标融入模型构建过程,唯有如此,才能充分发挥人工智能在加速药物研发中的潜力。
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-08-08,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

